Hyperbar iltbehandling for langvarig Coronavirus-sygdom-19: en sagsrapport
Baggrund
Pandemien med coronavirus sygdom 2019 (COVID-19) har resulteret i en voksende befolkning af individer, som oplever en bred vifte af langvarige symptomer efter bedring fra den akutte sygdom, refereret til med flere udtryk, herunder "post-COVID-tilstande" og "lange COVID." De fem mest almindelige symptomer, der er kendt efter COVID, er træthed (58%), hovedpine (44%), kognitiv svækkelse (27%), hårtab (25%) og dyspnø (24%) [1]. To vigtigste biologiske følgesygdomme af COVID-19 spiller roller i patogenesen af langvarig COVID. Den første er hyperkoagulabilitetstilstand karakteriseret ved øget risiko for okklusion af små og store kar [2]. Det andet er en ukontrolleret kontinuerlig inflammatorisk reaktion [3]. Mikroinfarkter og neuroinfamation er vigtige årsager til hjernehypoxi og kan være ansvarlige for det kroniske uafvendelige neurokognitive fald hos patienter med langvarig COVID [4]. En af mulighederne for at vende hypoxi, reducere neuroinfamation og inducere neuroplasticitet er hyperbar oxygenterapi (HBOT) [5].
I denne artikel præsenterer vi den første caserapport om tidligere raske, atletiske individer, der led af langvarigt post-COVID-syndrom, som blev behandlet med succes med HBOT.
Case præsentation
En 55-årig tidligere rask kaukasisk mand, der lider af vedvarende uafbrudte symptomer på langvarig COVID, besøgte vores klinik til evaluering. Den kliniske præsentation omfattede hukommelsesproblemer, forværring af multitasking-evner, træthed, lav energi, åndenød og nedsat fysisk behag, som alle startede efter akut SARS-CoV-2-infektion diagnosticeret 3 måneder før. Han udviklede oprindeligt højgradig feber uden brystsmerter, hoste eller åndenød den 21. januar 2021. Han blev indlagt på hospitalet på grund af dehydrering den 30. januar 2021 og blev diagnosticeret med COVID-19 ved omvendt transkription polymerase-kædereaktion ( RT-PCR). Under hospitalsopholdet udviklede han akut respiratorisk syndrom på grund af lungebetændelse og krævede støttende behandling med high-fow ilt i 1 uge. Han blev udskrevet fra hospitalet den 16. februar 2021. Ved udskrivelsen var han stabil med normal ilt, og der blev ikke konstateret neurologiske mangler ved fysisk undersøgelse. Derudover udviklede han 6 uger efter at være blevet diagnosticeret med COVID-19 en lungeemboli og blev behandlet med rivaroxaban. Før SARS-CoV-2-infektionen havde han været et sundt, velfungerende og atletisk individ.
Baseline-evalueringen udført på vores klinik, 3 måneder efter den akutte infektion, omfattede hjernemagnetisk resonansbilleddannelse (MRI) med perfusions- og difusionstensor-billeddannelse (DTI), computerstyret neurokognitiv evaluering, kardiopulmonal træningstest (CPET) og lungefunktionstests .
Ved baseline klagede patienten over åndenød ved træning samt hukommelsesbesvær og multitasking, der startede efter hans COVID-19 sygdom.
Fysisk og neurologisk undersøgelse var normal. Hjerne-MR-evaluering viste reduceret perfusion, der korrelerede med det kognitive fald som beskrevet nedenfor. Han blev henvist til hyperbar iltbehandling (HBOT), der omfattede 60 sessioner, 5 dage om ugen. Hver session inkluderede eksponering for 90 minutter med 100 % oxygen ved 2 atmosfærer absolut med 5 minutters luftpauser hvert 20. minut.
Patienten startede sin første HBOT den 19. april 2021 og afsluttede den 15. juli 2021 uden nogen væsentlige bivirkninger. Efter de første fem sessioner rapporterede han, at hans vejrtrækning var begyndt at blive bedre, og at han ikke længere havde muskelsmerter efter træning. Efter 15 sessioner bemærkede han mindre træthed og en forbedring i hans tidligere lave energi. Efter 20 sessioner bemærkede han, at hans åndedræts- og træningskapacitet var vendt tilbage til hans kapacitet før SARS-CoV-2-infektion og vendte tilbage til at løbe bjergstier. Derudover bemærkede han, at hans hukommelse og multitasking-evne vendte tilbage til hans præ-COVID-19-niveauer.
Den baseline hjerne-MRI, før HBOT, viste to små foci af signalændringer i højre og venstre parietale regioner, hvilket tyder på tidlig sygdom i små kar. Derudover var der et globalt fald i hjernegennemstrømningen. Som beskrevet detaljeret i fig. 1 og tabel 1 afslørede re-evaluering efter HBOT (udført 4 uger efter den sidste HBOT for at undgå enhver potentiel mellemeffekt) en signifikant stigning i hjerneperfusion. Tabel 2 og 3 viser forbedringerne i hjernens mikrostruktur som påvist ved MR-DTI.
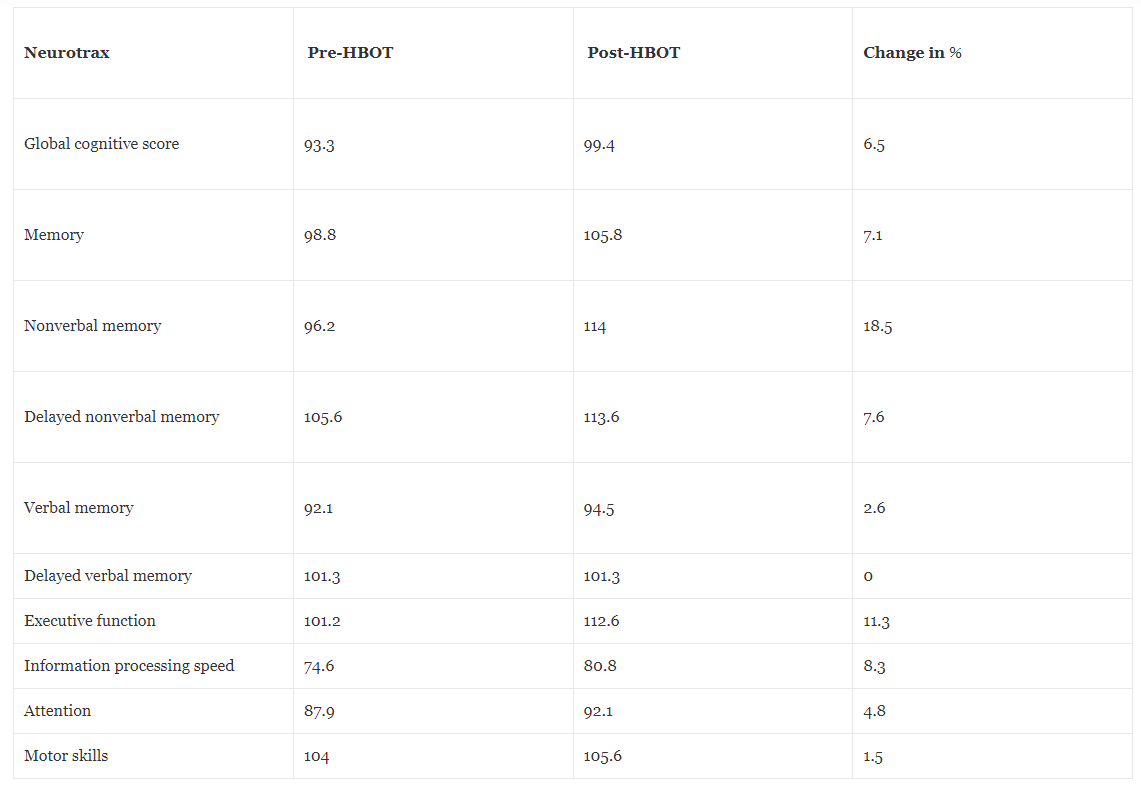
Neurokognitiv vurdering blev udført ved hjælp af NeuroTrax fuld computeriseret testbatteri til at måle forskellige aspekter af hjernefunktion, såsom hukommelse, informationsbehandlingshastighed, opmærksomhed og eksekutiv funktion, blev udført før og efter HBOT. Den neurokognitive test efter HBOT viste signifikant forbedring i global hukommelse, hvor den mest dominerende effekt var på nonverbal hukommelse, eksekutive funktioner, opmærksomhed, informationsprocessionshastighed, kognitiv fleksibilitet og multitasking. Tabel 4 opsummerer præ- og post-HBOT-scorerne i de forskellige kognitive domæner.
Den fysiske kapacitet blev evalueret ved hjælp af en maksimal kardiopulmonal træningstest (CPET) udført på et COSMED-løbebånd ved brug af Boston 5-protokollen. Tabel 5 viser de præ- og post-HBOT fysiologisk evaluerede parametre. Som beskrevet i detaljer var der en stigning på 34 % i VO2 max fra 3083 til 4130 ml pr. minut efter HBOT. Den forcerede vitale kapacitet (FVC) forbedredes med 44 % fra 4.76 til 6.87 L, det forcerede udåndingsvolumen (FEV) med 23 % fra 3.87 til 4.76 L og peak flow-måling (PEF) med 20.2 % fra 10.17 til 12.22 L pr. .
Efter at have modtaget fuld information i slutningen af sin post-HBOT-evaluering, underskrev patienten et informeret samtykke, der tillod offentliggørelse af hans medicinske information.
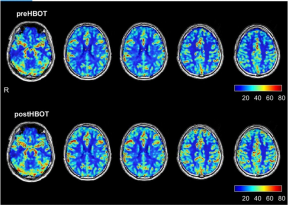
Fig 1Magnetisk resonansbilleddannelse af hjerneperfusion før og efter hyperbar iltbehandling. Den øverste række repræsenterer hjerneperfusion 3 måneder efter den akutte infektion, før hyperbar iltbehandling. Den nederste række repræsenterer perfusionsmagnetisk resonansbilleddannelse udført efter fuldførelse af hyperbar iltbehandlingsprotokollen.
Tabel 1Ændringer i hjernens blodstrøm før og efter hyperbar iltbehandling
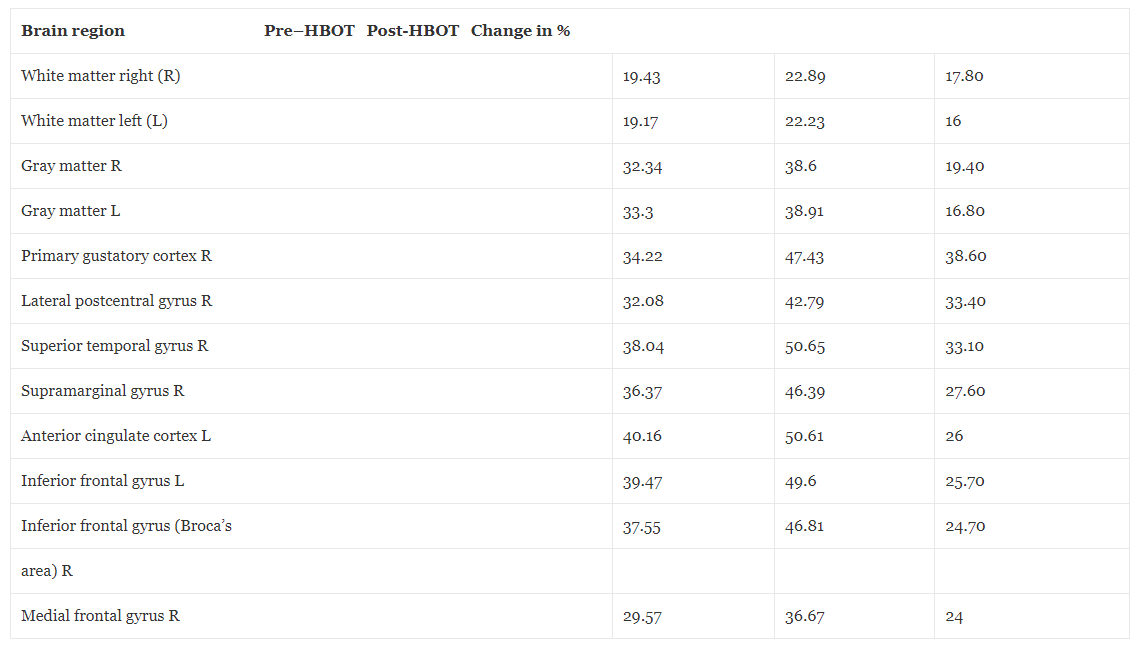
Diskussion og konklusioner
Her rapporterer vi det første tilfælde af en patient med langvarig COVID med kognitive og kardiorespiratoriske symptomer behandlet med succes af HBOT. Efter behandling viste han betydelige forbedringer i hjerneperfusion, hvid stofs hjernemikrostruktur og kognitiv og kardiopulmonal funktion. Denne case-rapport viser, at HBOT har potentiel brug til behandling af patienter med langvarig COVID, som lider af konstant kognitiv og fysisk funktionsnedgang.
Hypoxi spiller en vigtig rolle i patofysiologien af langvarig COVID. Systemisk hypoxi kan skyldes lungesvigt, og organrelateret hypoxi kan udvikle sig på grund af vaskulær skade. Vedvarende lungefunktion
Tabel 2Magnetisk resonansbilleddannelse – difusionstensorbilleddannelse fraktioneret anisotropi før og efter hyperbar iltbehandling

Fraktioneret anisotropi (FA) er et mål, der bruges til at evaluere hvidt stofs integritet, retningsbestemmelse og orden. En højere værdi af FA indikerer bedre fberorganisering. DTI difusion tensor billeddannelse
Tabel 3Magnetisk resonansbilleddannelse – difusionstensorbilleddannelse betyder difusivitetsændringer før og efter hyperbar iltbehandling
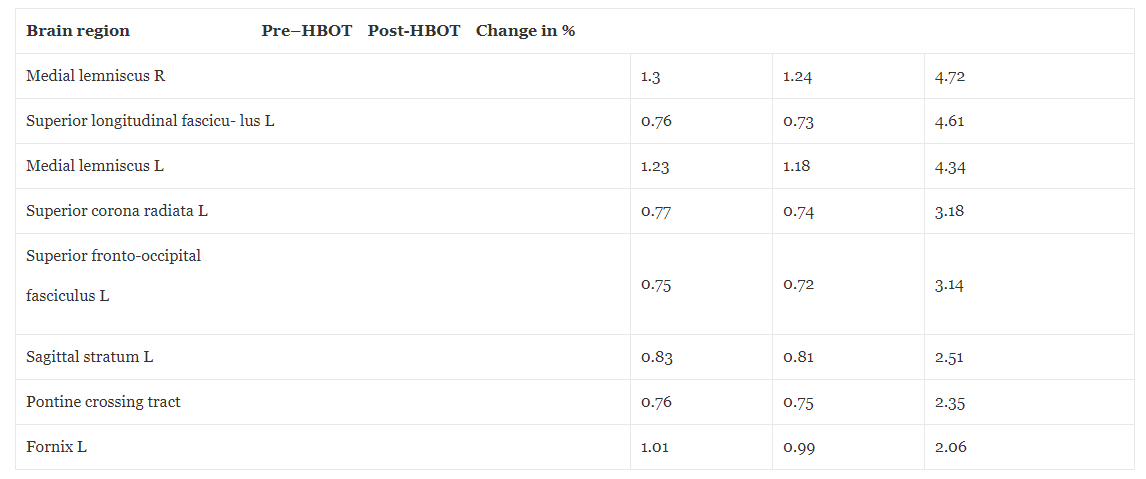
Middeldifusivitet (MD) er et mål, der bruges til at evaluere hvidt stofs fibertæthed. En lavere værdi for MD indikerer en højere tæthed. DTI difusion tensor billeddannelse.
Tabel 4Kognitive resultater før og efter hyperbar iltbehandling
Tabel 5Fysiologiske parametre før og efter hyperbar iltbehandling
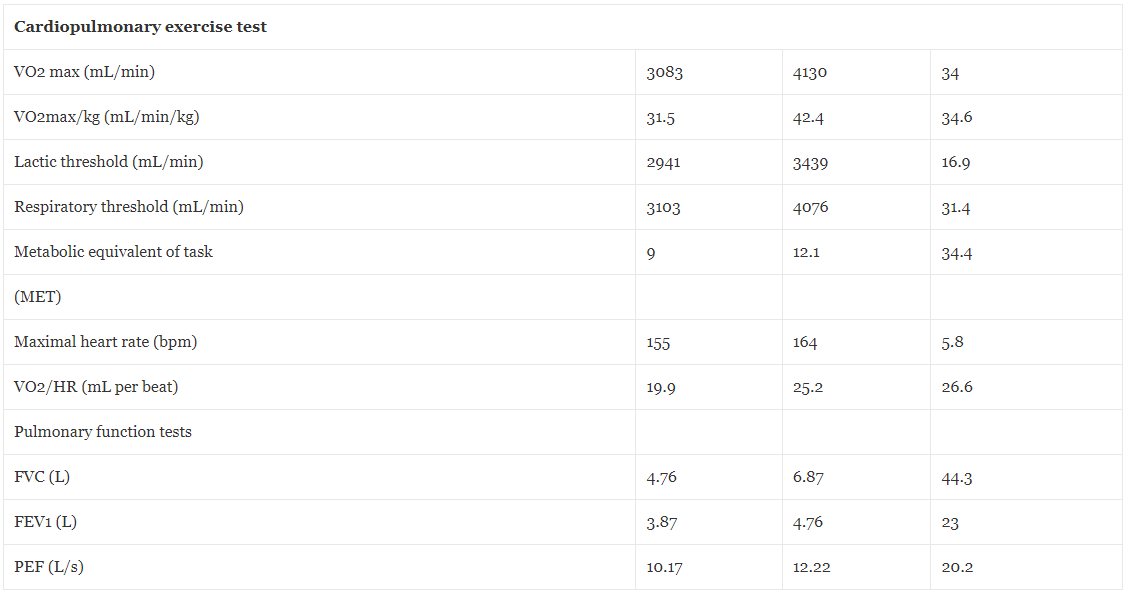
VO2max maksimal mængde ilt forbrugt under træning, ml/min milliliter per minut, VO2max/kg maksimal rate af ilt forbrugt under træning per kilogram, ml/min/Kg milliliter per minut per kilogram, MET metabolisk ækvivalent til opgave, slag/min hjerteslag per minut , VO2/HR rate af ilt forbrugt pr. hjertefrekvens, FVC tvungen vital kapacitet, L liter, FEV1 tvungen ekspiratorisk volumen, PEF peak flow måling, L/s liter pr. sekund.
svækkelse er set hos patienter, som havde behov for supplerende ilt under akut SARS-CoV-2-infektion selv 6 og 12 måneder efter den akutte infektion [6]. Da hjernefunktionalitet og regenerativ kapacitet er følsom over for ethvert fald i iltforsyningen [7], korrelerer langsigtede kognitive defekter med mængden af ilt, der er nødvendig for at overvinde åndedrætsbesværene [1]. Med hensyn til organrelateret iskæmi inducerede COVID-19 endotelskade og hyperkoagulation, hvilket øger risikoen for vaskulær dysfunktion, der er ansvarlig for den høje forekomst af myokardieinfarkt, iskæmisk slagtilfælde og lungeemboli [8]. I det forelagte tilfælde krævede patienten understøttende behandling med højt tilført oxygen i 1 uge under den akutte sygdom, hvilket betyder, at han havde lidt af systemisk hypoxi med deraf følgende risiko for langvarig kognitiv svækkelse på grund af anoksisk hjerneskade. Desuden udviklede han 6 uger efter den akutte infektion en lungeemboli, der var repræsentativ for den endoteliale dysfunktion med yderligere eksponering for systemisk hypoxi. Derudover havde han, som påvist ved hjerneperfusions-MR, mikrovaskulære perfusionsdefekter, der korrelerede med hans neurokognitive tilbagegang.
HBOT involverer indånding af 100 % ilt ved tryk, der overstiger 1 atmosfære absolut (ATA), hvilket øger mængden af ilt, der er opløst i kroppens væv. Selvom mange af de gavnlige virkninger af HBOT kan forklares ved forbedring af vævsiltningen, er det nu underforstået, at den kombinerede virkning af hyperoksi og hyperbarisk tryk udløser både ilt- og trykfølsomme gener, hvilket resulterer i induktion af regenerativ processer, herunder stamcelleproliferation og mobilisering med anti-apoptotiske og anti-inflammatoriske faktorer, angiogenese og neurogenese [9-12]. HBOT kan inducere neuroplasticitet og forbedre kognitiv funktion selv år efter den akutte fornærmelse [13]. I tilfældet med langvarig COVID, forbedrede HBOT cerebral blodtilførsel til de fejlperfunderede hjerneregioner (indikerende hjerneangiogenese) og forbedrede integriteten af hjernens mikrostruktur (indikerende neurogenese). Korrelationen mellem de signifikante forbedringer, der er påvist på hjernebilleddannelse og de neurokognitive forbedringer, indikerer, at de fleste af de gavnlige virkninger af HBOT faktisk er relateret til dets evne til at inducere neuroplasticitet i hjernens dysfunktionelle regioner.
HBOT har vist sig at have gavnlige virkninger på mitokondriefunktion, et afgørende element i passende muskelfunktion [12]. HBOT kan også øge antallet af prolifererende og differentierende satellitceller såvel som antallet af regenererede muskelfibre og fremme muskelstyrken [14]. Den nyligt intermitterende gentagne HBOT-protokol blev vist at have potentialet til at forbedre lungefunktionen med hensyn til peak ekspiratorisk fow (PEF) og force vital capacite (FVC) [15]. Hos den præsenterede patient blev ydeevnen af det kardiopulmonale system evalueret ved hjælp af kardiopulmonal træningstest (CPET) og lungefunktionstest. HBOT inducerede en signifikant forbedring på 34% i den maksimale iltforbrugskapacitet, en forbedring på 34.4% i de maksimale MET'er og en stigning på 16.9% i mælketærsklen. Med hensyn til lungefunktionen blev FVC forbedret med 44.3 % og PEF med 20.2 %. Disse målbare forbedringer korrelerede med patientens evne til at genvinde sin tidligere høje atletiske præstation.
I dette rapporterede tilfælde blev HBOT påbegyndt mere end 3 måneder efter den akutte SARS-CoV-2-infektion. Selvom symptomerne varede, indtil HBOT blev påbegyndt, og en betydelig bedring først begyndte, efter at HBOT var påbegyndt, er det muligt, at i det mindste noget af den kliniske forbedring kunne være sket uden HBOT. Imidlertid understøtter den pludselige markante forbedring med fuld bedring efter symptomernes kroniske karakter, vores forståelse af de fysiologiske effekter af HBOT og de objektive målinger på denne patient forholdet mellem behandlingen og de set forbedringer. Da dette kun er en case-rapport, er der behov for yderligere prospektive kliniske forsøg for at få en bedre forståelse af de potentielle gavnlige virkninger af HBOOT for patienter med langvarig COVID-XNUMX.
Sammenfattende repræsenterer denne artikel den første caserapport, der viser, at langvarig COVID kan behandles med HBOT. Den gavnlige effekt af HBOT kaster yderligere lys over patofysiologien af dette syndrom. Da dette er en enkelt case-rapport, er yderligere prospektive randomiserede kontrolundersøgelser nødvendige for brugen af hyperbar iltterapi til behandling af langvarig COVID.
Forkortelser
HBOT: Hyperbar iltbehandling; MRI: Magnetisk resonansbilleddannelse; DTI: Dif- fusionstensorbilleddannelse; VO2 max: Maksimal mængde ilt forbrugt under træning; CPET: Kardiopulmonal træningstest; HR: Puls; Bpm: Hjerteslag pr. minut; FVC: Forceret vital kapacitet; FEV1: Forceret ekspiratorisk volumen; PEF: Peak flow-måling.
Anerkendelser
Ikke anvendelig.
Forfatterens bidrag
AMB, ES, SE og SK analyserede og fortolkede patientdataene vedrørende MR, perfusion og DTI. AMB og SE analyserede og fortolkede patientdataene vedrørende hjerte-lunge- og lungefunktionstestene. Alle forfattere læste og godkendte det endelige manuskript.
Forfatterens bidrag
AMB, ES, SE og SK analyserede og fortolkede patientdataene vedrørende MR, perfusion og DTI. AMB og SE analyserede og fortolkede patientdataene vedrørende hjerte-lunge- og lungefunktionstestene. Alle forfattere læste og godkendte det endelige manuskript.
Tilgængelighed af data og materialer
Alle data genereret eller analyseret i løbet af denne undersøgelse er inkluderet i denne publicerede artikel.
erklæringer
Etik godkendelse og samtykke til at deltage
Ikke anvendelig.
Samtykke til offentliggørelse
Der blev indhentet skriftligt informeret samtykke fra patienten til offentliggørelse af denne case-rapport og eventuelle medfølgende billeder. En kopi af det skriftlige samtykke er tilgængeligt til gennemsyn af dette tidsskrifts chefredaktør.
Konkurrerende interesser
AMB, ZW, SK, MG og UQ arbejder for AVIV Clinics. ES arbejder for AVIV Scientifc LTD. SE er medstifter og aktionær hos AVIV Scientifc LTD.
Modtaget: 11. oktober 2021 Accepteret: 21. januar 2022, Udgivet online: 15. februar 2022
Referencer
Lopez-Leon S, et al. Mere end 50 langsigtede effekter af COVID-19: en systematisk gennemgang og metaanalyse. Sci Rep. 2021;11(1):16144.
LeviM, et al. Koagulationsabnormiteter og trombose hos patienter med COVID-19. Lancet hæmatol. 2020;7(6):e438–40.
MahmudpourM, et al. COVID-19 cytokinstorm: inflammations vrede. Cytokin. 2020;133: 155151.
LiB, et al. Hjerne-immune interaktioner ved perinatal hypoxisk-iskæmisk hjerneskade. Prog Neurobiol. 2017;159:50–68.
ShapiraR, et al. Hyperbar oxygenterapi forbedrer patofysiologien af 3xTg-AD musemodel ved at dæmpe neuroinfamation. Neurobiol aldring. 2018;62:105–19.
HuangL, et al. 1-års resultater hos hospitalsoverlevere med COVID-19: et longitudinelt kohortestudie. Lancet. 2021;398(10302):747-58.
HadannyA, Efrati S. Oxygen - en begrænsende faktor for hjernegendannelse. Crit Care. 2015;19:307.
KatsoularisI, et al. Risiko for akut myokardieinfarkt og iskæmisk slagtilfælde efter COVID-19 i Sverige: en selvkontrolleret case-serie og matchet kohorteundersøgelse. Lancet. 2021;398(10300):599-607.
Pena-VillalobosI, et al. Hyperbar oxygen øger stamcelleproliferation, angiogenese og sårhelende evne hos WJ-MSC'er i diabetiske mus. Front Physiol. 2018;9:995.
CabigasBP, et al. Hyperoxisk og hyperbar-induceret kardiobeskyttelse: rolle af nitrogenoxidsyntase 3. Cardiovasc Res. 2006;72(1):143–51.
GregorevicP, Lynch GS, Williams DA. Hyperbar oxygen modulerer antioxidant enzymaktivitet i rottes skeletmuskler. Eur J Appl Physiol. 2001;86(1):24–7.
ZhouZ, et al. Beskyttelse af mitokondriel funktion og forbedring af kognitiv genopretning hos rotter behandlet med hyperbar oxygen efter lateral fuid-percussion-skade. J Neurokirurgi. 2007;106(4):687-94.
HadannyA, et al. Hyperbar iltbehandling forbedrer neurokognitive funktioner hos patienter efter slagtilfælde - en retrospektiv analyse. Restor Neurol Neurosci. 2020;38(1):93-107.
HorieM, et al. Forbedring af satellitcelledifferentiering og funktionel genopretning i skadet skeletmuskulatur ved hyperbar iltbehandling. J Appl Physiol. 2014;116(2):149–55.
HadannyA, et al. Hyperbar iltbehandlingseffekter på lungefunktioner: en prospektiv kohorteundersøgelse. BMC Pulm Med. 2019;19(1):148.
Forlagets note
Springer Nature forbliver neutral med hensyn til jurisdiktionskrav i offentliggjorte kort og institutionelle tilknytninger.






