Hyperbar oksygenbehandling for langvarig koronavirussykdom-19: en saksrapport
Bakgrunn
Pandemien med koronavirussykdom 2019 (COVID-19) har resultert i en voksende populasjon av individer som opplever et bredt spekter av langvarige symptomer etter bedring fra den akutte sykdommen, referert til med flere begreper, inkludert "post-COVID-tilstander" og "lange" COVID." De fem vanligste symptomene som er kjent etter COVID er tretthet (58 %), hodepine (44 %), kognitiv svikt (27 %), hårtap (25 %) og dyspné (24 %) [1]. To viktige biologiske følgetilstander av COVID-19 spiller roller i patogenesen til langvarig COVID. Det første er hyperkoagulabilitet preget av økt risiko for okklusjon av små og store kar [2]. Det andre er en ukontrollert kontinuerlig inflammatorisk respons [3]. Mikroinfarkter og nevrobetennelse er viktige årsaker til hjernehypoksi og kan være ansvarlige for den kroniske uavlatelige nevrokognitive nedgangen hos pasienter med langvarig COVID [4]. Et av alternativene for å reversere hypoksi, redusere nevrobetennelse og indusere nevroplastisitet er hyperbar oksygenbehandling (HBOT) [5].
I denne artikkelen presenterer vi den første kasusrapporten om tidligere friske, atletiske individer som led av langvarig post-COVID-syndrom behandlet med HBOT.
Saksframlegg
En 55 år gammel tidligere frisk kaukasisk mann som led av vedvarende uopphørlige symptomer på langvarig COVID, besøkte klinikken vår for evaluering. Den kliniske presentasjonen inkluderte hukommelsesproblemer, forverring av multitasking-evner, tretthet, lav energi, pustløshet og redusert fysisk behag, som alle startet etter akutt SARS-CoV-2-infeksjon diagnostisert 3 måneder før. Han utviklet opprinnelig høygradig feber uten brystsmerter, hoste eller kortpustethet, 21. januar 2021. Han ble innlagt på sykehus på grunn av dehydrering 30. januar 2021 og ble diagnostisert med COVID-19 ved omvendt transkripsjon av polymerasekjedereaksjon ( RT-PCR). Under sykehusoppholdet utviklet han akutt respiratorisk syndrom på grunn av lungebetennelse og trengte støttende behandling med oksygen i 1 uke. Han ble utskrevet fra sykehus 16. februar 2021. Ved utskrivning var han stabil med normalt oksygen og det ble ikke påvist nevrologiske mangler ved fysisk undersøkelse. I tillegg, 6 uker etter å ha blitt diagnostisert med COVID-19, utviklet han en lungeemboli og ble behandlet med rivaroksaban. Før SARS-CoV-2-infeksjonen hadde han vært et sunt, høytfungerende og atletisk individ.
Baseline-evalueringen gjort ved vår klinikk, 3 måneder etter den akutte infeksjonen, inkluderte magnetisk resonansavbildning av hjernen (MRI) med perfusjon og difusjonstensoravbildning (DTI), datastyrt nevrokognitiv evaluering, kardiopulmonal treningstest (CPET) og lungefunksjonstester. .
Ved baseline klaget pasienten over kortpustethet med trening samt problemer med hukommelse og multitasking som startet etter hans COVID-19-sykdom.
Fysisk og nevrologisk undersøkelse var normal. Hjerne-MR-evaluering viste redusert perfusjon som korrelerte med den kognitive nedgangen som beskrevet nedenfor. Han ble henvist til hyperbar oksygenbehandling (HBOT) som inkluderte 60 økter, 5 dager i uken. Hver økt inkluderte eksponering for 90 minutter med 100 % oksygen ved 2 atmosfærer absolutt med 5-minutters luftpauser hvert 20. minutt.
Pasienten startet sin første HBOT 19. april 2021 og avsluttet 15. juli 2021 uten noen vesentlige bivirkninger. Etter de første fem øktene rapporterte han at pusten hadde begynt å bli bedre og at han ikke lenger hadde muskelsmerter etter trening. Etter 15 økter bemerket han mindre tretthet og en forbedring i sin tidligere lave energi. Etter 20 økter la han merke til at puste- og treningskapasiteten hans var tilbake til kapasiteten før SARS-CoV-2-infeksjon, og gikk tilbake til løpende fjellstier. I tillegg bemerket han at hukommelsen og multitasking-evnen hans kom tilbake til nivåene før COVID-19.
Baseline hjerne-MR, før HBOT, viste to små foci av signalendringer i høyre og venstre parietalregioner som tyder på tidlig småkarsykdom. I tillegg var det en global reduksjon i hjernens perfusjon. Som beskrevet i figur 1 og tabell 1, avslørte re-evaluering etter HBOT (utført 4 uker etter siste HBOT for å unngå potensiell mellomeffekt) en signifikant økning i hjerneperfusjon. Tabell 2 og 3 presenterer forbedringene i hjernens mikrostruktur som demonstrert av MR-DTI.
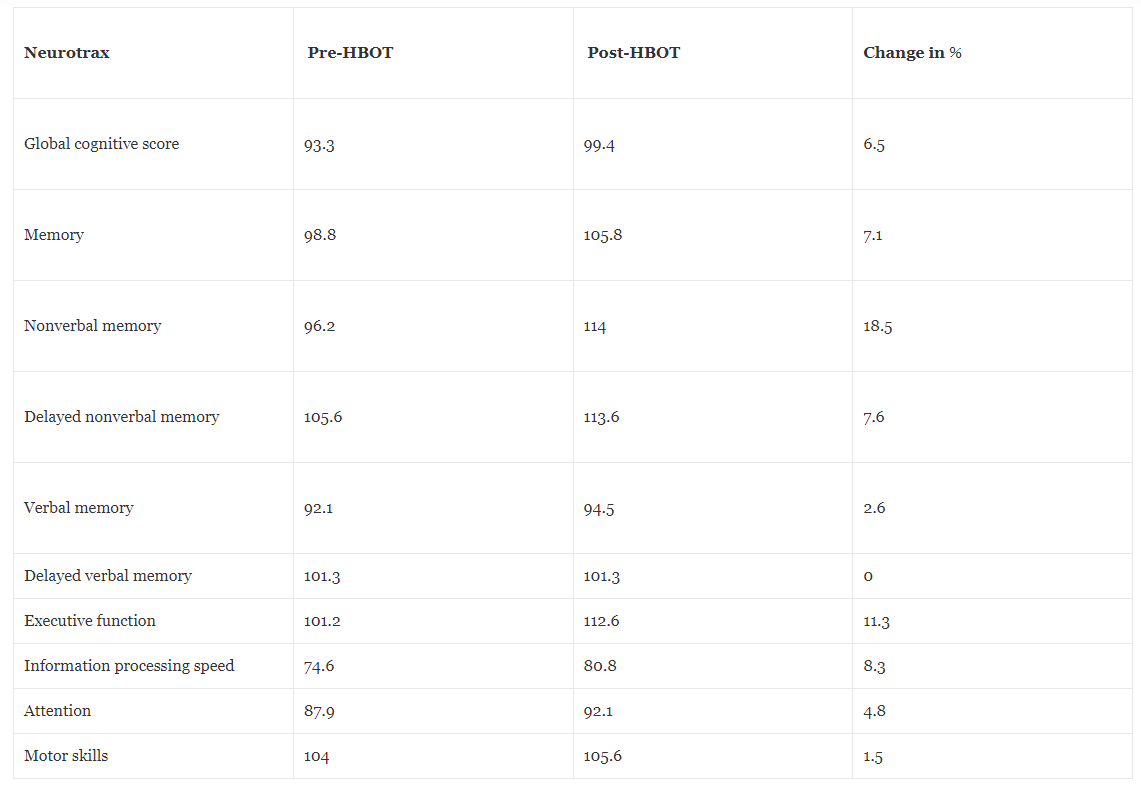
Nevrokognitiv vurdering ble gjort ved å bruke NeuroTrax fullstendig datastyrt testbatteri for å måle forskjellige aspekter av hjernefunksjonen, som minne, informasjonsbehandlingshastighet, oppmerksomhet og eksekutiv funksjon, ble gjort før og etter HBOT. Den post-HBOT nevrokognitive testingen viste betydelig forbedring i globalt minne, med den mest dominerende effekten på ikke-verbal hukommelse, eksekutive funksjoner, oppmerksomhet, informasjonsprosesjonshastighet, kognitiv fleksibilitet og multitasking. Tabell 4 oppsummerer pre- og post-HBOT-skårene i de forskjellige kognitive domenene.
Fysisk kapasitet ble evaluert ved maksimal kardiopulmonal treningstest (CPET) utført på en COSMED tredemølle ved bruk av Boston 5-protokollen. Tabell 5 viser de fysiologiske evaluerte parametrene før og etter HBOT. Som beskrevet i detalj var det en økning på 34 % i VO2-maks fra 3083 til 4130 ml per minutt etter HBOT. Den tvungne vitale kapasiteten (FVC) ble forbedret med 44 % fra 4.76 til 6.87 l, det tvungne ekspirasjonsvolumet (FEV) med 23 % fra 3.87 til 4.76 l, og toppstrømmåling (PEF) med 20.2 % fra 10.17 til 12.22 l per sekund .
Etter å ha mottatt full informasjon på slutten av sin post-HBOT-evaluering, signerte pasienten et informert samtykke som tillot publisering av sin medisinske informasjon.
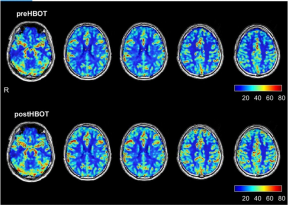
Fig. 1Magnetisk resonansavbildning av hjerneperfusjon før og etter hyperbar oksygenbehandling. Den øverste raden representerer hjerneperfusjon 3 måneder etter den akutte infeksjonen, før hyperbar oksygenbehandling. Den nedre raden representerer perfusjonsmagnetisk resonansavbildning utført etter å ha fullført protokollen for hyperbar oksygenbehandling.
Tabell 1Hjerneblodstrømmen endres før og etter hyperbar oksygenbehandling
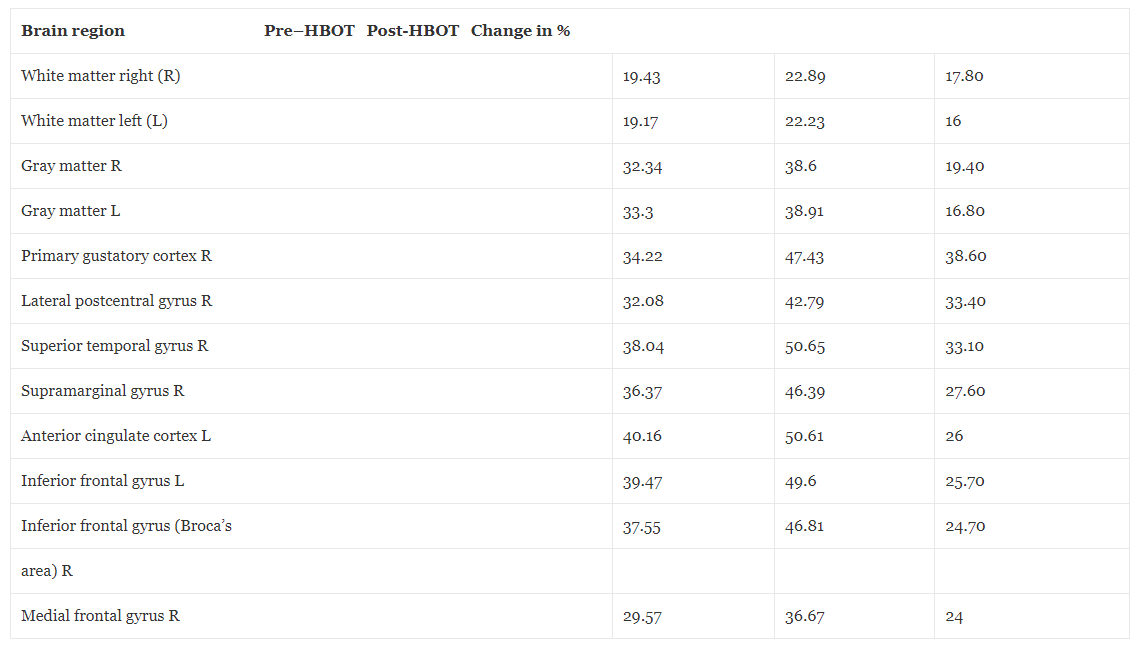
Diskusjon og konklusjoner
Her rapporterer vi det første tilfellet av en pasient med langvarig COVID med kognitive og kardiorespiratoriske symptomer behandlet med suksess av HBOT. Etter behandlingen viste han betydelige forbedringer i hjerneperfusjon, hvit substans hjernemikrostruktur og kognitiv og kardiopulmonal funksjon. Denne kasusrapporten viser at HBOT har potensiell bruk for behandling av pasienter med langvarig covid som lider av uopphørlig kognitiv og fysisk funksjonsnedgang.
Hypoksi spiller en viktig rolle i patofysiologien til langvarig COVID. Systemisk hypoksi kan skyldes lungesvikt, og organrelatert hypoksi kan utvikles på grunn av vaskulær skade. Vedvarende lungefunksjon
Tabell 2Magnetisk resonansavbildning – difusjonstensoravbildning fraksjonelle anisotropi-endringer før og etter hyperbar oksygenbehandling

Fraksjonell anisotropi (FA) er et mål som brukes til å evaluere hvitt stoffs integritet, retning og rekkefølge. En høyere verdi på FA indikerer bedre organisasjon. DTI-difusjonstensoravbildning
Tabell 3Magnetisk resonansavbildning – difusjonstensoravbildning betyr difusivitetsendringer før og etter hyperbar oksygenbehandling
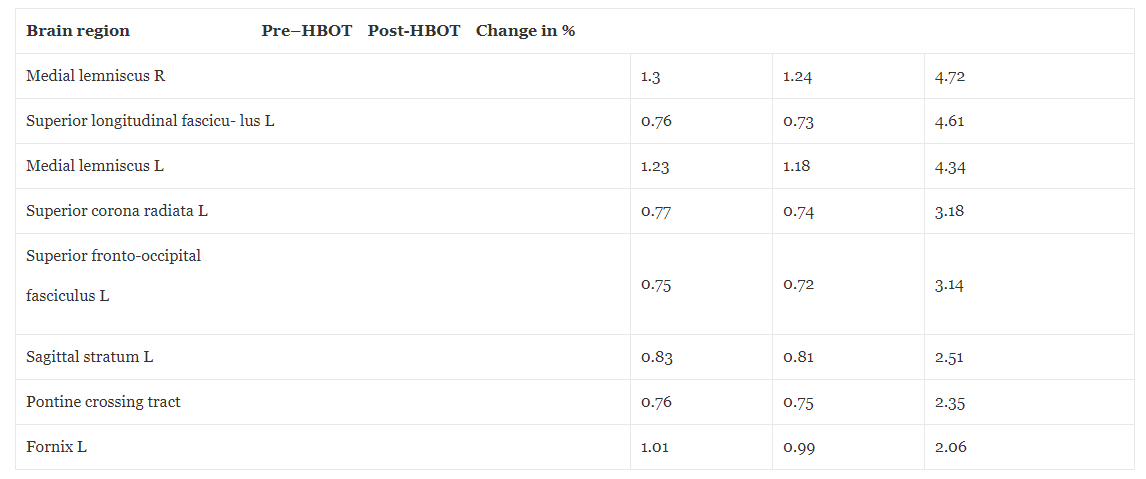
Gjennomsnittlig diffusivitet (MD) er et mål som brukes til å evaluere fibertetthet i hvitt stoff. En lavere verdi på MD indikerer en høyere tetthet. DTI-difusjonstensoravbildning.
Tabell 4Kognitive skårer før og etter hyperbar oksygenbehandling
Tabell 5Fysiologiske parametere før og etter hyperbar oksygenbehandling
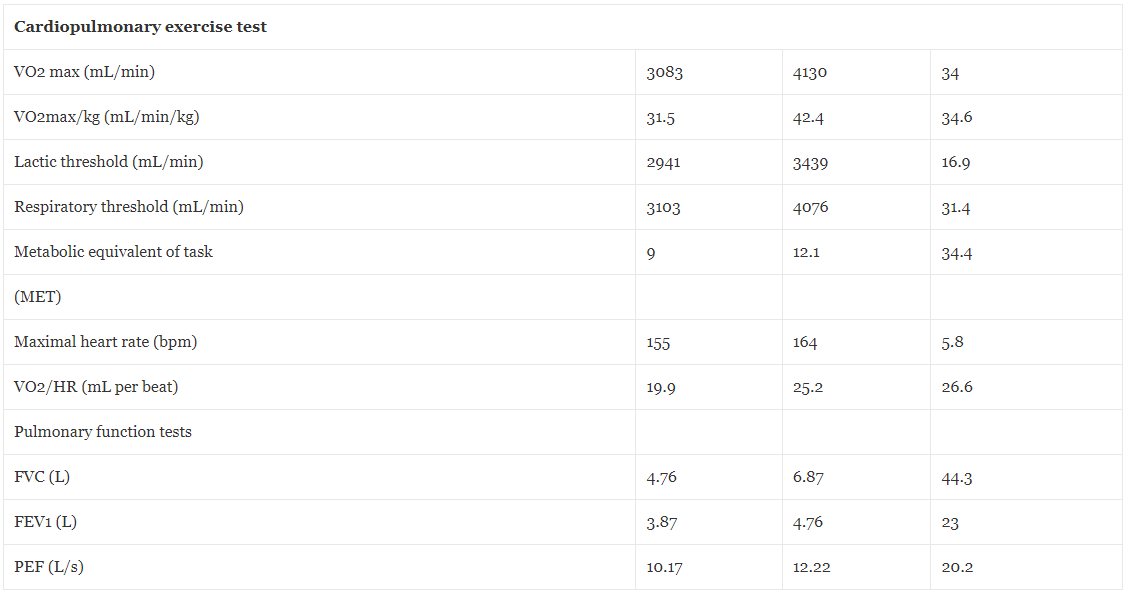
VO2max maksimal hastighet av oksygen forbrukt under trening, ml/min milliliter per minutt, VO2max/kg maksimal rate av oksygen forbrukt under trening per kilogram, ml/min/Kg milliliter per minutt per kilogram, MET metabolsk ekvivalent av oppgaven, slag per minutt hjerteslag per minutt , VO2/HR rate av oksygen forbrukt per hjertefrekvens, FVC tvungen vitalkapasitet, L liter, FEV1 tvungen ekspirasjonsvolum, PEF peak flow måling, L/s liter per sekund.
svekkelse har blitt sett hos pasienter som trengte ekstra oksygen under akutt SARS-CoV-2-infeksjon selv 6 og 12 måneder etter den akutte infeksjonen [6]. Siden hjernefunksjonalitet og regenerativ kapasitet er følsom for enhver nedgang i oksygentilførsel [7], korrelerer langsiktige kognitive mangler med mengden oksygen som trengs for å overvinne åndedrettsvansker [1]. Når det gjelder organrelatert iskemi, induserte COVID-19 endotelskade og hyperkoagulasjon, noe som øker risikoen for vaskulær dysfunksjon som er ansvarlig for den høye forekomsten av hjerteinfarkt, iskemisk slag og lungeemboli [8]. I det presenterte tilfellet trengte pasienten støttende behandling med oksygen med høyt tilskudd i 1 uke under den akutte sykdommen, noe som betyr at han hadde lidd av systemisk hypoksi med påfølgende risiko for langvarig kognitiv svikt på grunn av anoksisk hjerneskade. I tillegg utviklet han 6 uker etter den akutte infeksjonen en lungeemboli, representativ for endoteldysfunksjonen med ytterligere eksponering for systemisk hypoksi. I tillegg, som demonstrert av hjerneperfusjons-MR, hadde han mikrovaskulære perfusjonsdefekter som korrelerte med hans nevrokognitive tilbakegang.
HBOT innebærer inhalering av 100 % oksygen ved trykk over 1 atmosfære absolutt (ATA), og øker dermed mengden oksygen som er oppløst i kroppsvevet. Selv om mange av de gunstige effektene av HBOT kan forklares med forbedring av vevsoksygenering, er det nå forstått at den kombinerte virkningen av hyperoksi og hyperbarisk trykk utløser både oksygen- og trykkfølsomme gener, noe som resulterer i induksjon av regenerativ prosesser inkludert stamcelleproliferasjon og mobilisering med anti-apoptotiske og anti-inflammatoriske faktorer, angiogenese og neurogenese [9-12]. HBOT kan indusere nevroplastisitet og forbedre kognitiv funksjon selv år etter den akutte fornærmelsen [13]. I tilfellet presentert med lang COVID, forbedret HBOT cerebral blodtilførsel til de misperfuserte hjerneregionene (indikerende på hjerneangiogenese) og forbedret integriteten til hjernens mikrostruktur (indikerende på neurogenese). Korrelasjonen mellom de betydelige forbedringene som er demonstrert på hjerneavbildning og de nevrokognitive forbedringene indikerer at de fleste av de fordelaktige effektene av HBOT faktisk er relatert til dens evne til å indusere nevroplastisitet i hjernens dysfunksjonelle regioner.
HBOT har vist seg å ha gunstige effekter på mitokondriell funksjon, et avgjørende element i passende muskelfunksjon [12]. HBOT kan også øke antall prolifererende og differensierende satellittceller samt antall regenererte muskelfibre, og fremme muskelstyrke [14]. Den nylig intermitterende gjentatte HBOT-protokollen ble vist å ha potensial til å forbedre lungefunksjonen med hensyn til peak ekspiratorisk fow (PEF) og force vital capacity (FVC) [15]. Hos den presenterte pasienten ble ytelseskapasiteten til det kardiopulmonale systemet evaluert ved å bruke kardiopulmonal treningstest (CPET) og lungefunksjonstester. HBOT induserte en signifikant forbedring på 34 % i den maksimale oksygenforbrukskapasiteten, en forbedring på 34.4 % i de maksimale MET-ene og en økning på 16.9 % i melketerskelen. Når det gjelder lungefunksjon, ble FVC forbedret med 44.3 %, og PEF med 20.2 %. Disse målbare forbedringene korrelerte med pasientens evne til å gjenvinne sin tidligere høye atletiske ytelse.
I dette rapporterte tilfellet ble HBOT initiert mer enn 3 måneder etter den akutte SARS-CoV-2-infeksjonen. Selv om symptomene vedvarte til HBOT ble initiert og betydelig bedring begynte først etter at HBOT ble initiert, er det mulig at i det minste noe av den kliniske forbedringen kunne ha skjedd uten HBOT. Imidlertid støtter den brå betydelige forbedringen med full bedring etter den kroniske karakteren av symptomene, vår forståelse av de fysiologiske effektene av HBOT og de objektive målingene som er gjort på denne pasienten forholdet mellom behandlingen og forbedringene som er sett. Siden dette kun er en kasusrapport, er det nødvendig med ytterligere prospektive kliniske studier for å få en bedre forståelse av de potensielle fordelaktige effektene av HBOOT for pasienter med langvarig COVID.
Oppsummert representerer denne artikkelen den første kasusrapporten som viser at lang COVID kan behandles med HBOT. Den fordelaktige effekten av HBOT kaster ytterligere lys over patofysiologien til dette syndromet. Siden dette er en enkelt case-rapport, er ytterligere prospektive randomiserte kontrollstudier nødvendig for bruk av hyperbar oksygenterapi ved behandling av langvarig COVID.
Forkortelser
HBOT: Hyperbar oksygenbehandling; MR: Magnetisk resonansavbildning; DTI: Diffusjonstensoravbildning; VO2 max: Maksimal oksygenmengde som forbrukes under trening; CPET: Kardiopulmonal treningstest; HR: Hjertefrekvens; Bpm: Hjerteslag per minutt; FVC: Forsert vital kapasitet; FEV1: Forsert ekspirasjonsvolum; PEF: Toppstrømmåling.
Takk til
Ikke aktuelt.
Forfatterens bidrag
AMB, ES, SE og SK analyserte og tolket pasientdataene angående MR, perfusjon og DTI. AMB og SE analyserte og tolket pasientdataene vedrørende hjerte- og lungefunksjonstestene. Alle forfattere leste og godkjente det endelige manuskriptet.
Forfatterens bidrag
AMB, ES, SE og SK analyserte og tolket pasientdataene angående MR, perfusjon og DTI. AMB og SE analyserte og tolket pasientdataene vedrørende hjerte- og lungefunksjonstestene. Alle forfattere leste og godkjente det endelige manuskriptet.
Tilgjengelighet av data og materialer
Alle data generert eller analysert i løpet av denne studien er inkludert i denne publiserte artikkelen.
erklæringer
Etikkgodkjenning og samtykke til å delta
Ikke aktuelt.
Samtykke til publisering
Det ble innhentet skriftlig informert samtykke fra pasienten for publisering av denne saksrapporten og eventuelle medfølgende bilder. En kopi av det skriftlige samtykket er tilgjengelig for vurdering av sjefredaktøren for dette tidsskriftet.
Konkurrerende interesser
AMB, ZW, SK, MG og UQ jobber for AVIV Clinics. ES jobber for AVIV Scientifc LTD. SE er medgründer og aksjonær i AVIV Scientifc LTD.
Mottatt: 11. oktober 2021 Godtatt: 21. januar 2022, publisert på nett: 15. februar 2022
Referanser
Lopez-Leon S, et al. Mer enn 50 langsiktige effekter av COVID-19: en systematisk gjennomgang og metaanalyse. Sci Rep. 2021;11(1):16144.
LeviM, et al. Koagulasjonsavvik og trombose hos pasienter med COVID-19. Lancet Haematol. 2020;7(6):e438–40.
MahmudpourM, et al. COVID-19 cytokinstorm: sinne ved betennelse. Cytokin. 2020;133: 155151.
LiB, et al. Hjerne-immune interaksjoner ved perinatal hypoksisk-iskemisk hjerneskade. Prog Neurobiol. 2017;159:50–68.
ShapiraR, et al. Hyperbar oksygenterapi forbedrer patofysiologien til 3xTg-AD-musemodellen ved å dempe nevroinfamasjon. Nevrobiol aldring. 2018;62:105–19.
HuangL, et al. 1-års utfall hos overlevende på sykehus med COVID-19: en longitudinell kohortstudie. Lancet. 2021;398(10302):747–58.
HadannyA, Efrati S. Oksygen - en begrensende faktor for hjernegjenoppretting. Crit Care. 2015;19:307.
Katsoularis I, et al. Risiko for akutt hjerteinfarkt og iskemisk hjerneslag etter COVID-19 i Sverige: en selvkontrollert kasusserie og matchet kohortstudie. Lancet. 2021;398(10300):599–607.
Pena-VillalobosI, et al. Hyperbar oksygen øker stamcelleproliferasjon, angiogenese og sårhelingsevne til WJ-MSCs hos diabetiske mus. Front Physiol. 2018;9:995.
CabigasBP, et al. Hyperoksisk og hyperbar-indusert kardiobeskyttelse: rollen til nitrogenoksidsyntase 3. Cardiovasc Res. 2006;72(1):143–51.
GregorevicP, Lynch GS, Williams DA. Hyperbar oksygen modulerer antioksidant enzymaktivitet i rotteskjelettmuskler. Eur J Appl Physiol. 2001;86(1):24–7.
ZhouZ, et al. Beskyttelse av mitokondriell funksjon og forbedring i kognitiv utvinning hos rotter behandlet med hyperbar oksygen etter lateral fuid-perkusjonsskade. J Nevrokirurgi. 2007;106(4):687–94.
HadannyA, et al. Hyperbar oksygenbehandling forbedrer nevrokognitive funksjoner hos pasienter etter hjerneslag - en retrospektiv analyse. Restor Neurol Neurosci. 2020;38(1):93–107.
HorieM, et al. Forbedring av satellittcelledifferensiering og funksjonell utvinning i skadet skjelettmuskulatur ved hyperbar oksygenbehandling. J Appl Physiol. 2014;116(2):149–55.
HadannyA, et al. Hyperbar oksygenbehandlingseffekter på lungefunksjoner: en prospektiv kohortstudie. BMC Pulm Med. 2019;19(1):148.
Utgiverens notat
Springer Nature forblir nøytral med hensyn til jurisdiksjonskrav i publiserte kart og institusjonelle tilknytninger.






